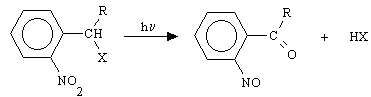
| 1. | Caged compounds |
1.1 Generalità
La strategia della rapida generazione fotochimica di composti
biologicamente attivi a partire da precursori fotosensibili e inattivi è un utile metodo
per sondare i meccanismi di processi biologici in sistemi cellulari o subcellulari
altamente organizzati. L'uso di composti fotoattivabili permette di superare i problemi
associati alla lenta diffusione del substrato entro i preparati biologici, rendendo
possibili misurazioni con elevata risoluzione temporale. Questa tecnica si sta inoltre
dimostrando valida per l'analisi di meccanismi enzimatici in associazione alla
cristallografia macromolecolare risolta nel tempo.
Nell'approccio fotochimico allo studio dei sistemi biologici, ha avuto inizialmente
notevole importanza l'uso di molecole fotoisomerizzabili, composti contenenti il gruppo
azobenzenico ed esistenti nelle forme cis e trans, rispetto al doppio legame
N=N [34]. Le due forme stereoisomere hanno caratteristiche differenti e sono
interconvertibili tra loro per effetto della luce. Composti di questo genere sono stati
principalmente impiegati come agonisti di recettori acetilcolinici, verso i quali le due
forme isomere hanno diversa affinità [55, 69], e come agenti leganti per cationi
bivalenti, con diversa capacità chelante nelle forme cis e trans [6].
Nell'ultimo decennio hanno assunto sempre maggior importanza specie chimiche fotolisabili,
in cui un gruppo di protezione è legato alla molecola di interesse (effettore) formando
un complesso biologicamente inattivo. Nella maggior parte di questi composti, denominati
fin dall'inizio del loro impiego "caged compounds" [49, 58], il gruppo di
protezione è costituito da un o-nitrobenzile [48, 57, 72]. Questi complessi in
seguito ad irraggiamento con luce ad una lunghezza d'onda compresa tra 300 e 400 nm
sottostanno ad una reazione ossido-riduttiva intramolecolare dando origine all'effettore
(HX o X-) e ad un nitrosoderivato come sottoprodotto:
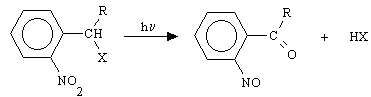
Spesso viene usato come gruppo di protezione il 1-(2-nitrofenil)etile
in quanto la presenza di un sostituente sul carbonio a ne
aumenta la sensibilità fotolitica; inoltre si forma come sottoprodotto il
2-nitrosobenzofenone che è meno reattivo della 2-nitrosobenzaldeide nei confronti dei
sistemi biologici. Il più vasto gruppo di effettori è costituito dal fosfato e da
nucleotidi ed altri esteri fosforici. Oltre a questi sono stati sintetizzati ed impiegati
in studi biologici derivati di acidi carbossilici, di alcoli, di ammine e di amminoacidi.
Derivati o-nitrobenzilici particolari sono i caged Ca++ nei quali il
gruppo protettore è legato ad un chelante del calcio (EDTA per il DM-nitrofen e BAPTA
(acido 1,2-bis-(2-amminofenossi)etano-N,N,N',N'-tetracetico) per la serie dei nitr) la cui
affinità per questo elemento viene ridotta fotoliticamente.
Un altro tipo di composti di notevole importanza sono i caged H+. Tutti i
derivati o-nitrobenzilici liberano un protone come prima fase della reazione
fotolitica; perché uno di questi sia utilizzabile come caged H+ è però
necessario che il gruppo successivamente rilasciato (X-) sia sufficientemente
acido da non legare nuovamente i protoni e non abbia particolari effetti biologici. Su
queste basi è stato sintetizzato e impiegato come caged H+ il
2-idrossifenil-1-(2-nitrofenil)etil fosfato.
Alcuni limiti dei derivati o-nitrobenzilici, quali la bassa velocità o resa
fotolitica di alcuni composti e la possibile tossicità dei sottoprodotti, hanno fatto sì
che recentemente si siano ricercati altri gruppi di protezione. Sono stati sintetizzati
diversi caged Pi [3]; in particolare il 3,5-dinitrofenil fosfato è stato impiegato in
studi sulla glicogeno fosforilasi. Buone prospettive sembrano inoltre offerte dai derivati
benzoinici dei quali sono stati ottenuti promettenti caged Pi, esteri fosforici [14, 27,
91] e carbossilici [82].
1.2 Sintesi
Nella sintesi dei caged compounds è possibile individuare un passaggio peculiare che consiste idealmente nella reazione di condensazione tra l'effettore ed il gruppo di protezione, anche se generalmente uno dei due gruppi, o entrambi, partecipano alla reazione in forma modificata. Nella pratica è inoltre possibile definire classi di effettori per i quali sia utilizzabile una analoga reazione di condensazione.
1.2.1 Composti acidi
Uno schema sintetico che può essere potenzialmente applicato ad un
grande numero di derivati o-nitrobenzilici di composti a carattere acido è stato
messo a punto alla fine degli anni '80. Si rifà ad un processo già utilizzato per
ottenere o-nitrobenzil-cAMP [24] ed è stato inizialmente impiegato per la sintesi
di alcuni caged nucleotidi [98].
Il prodotto finale si ottiene dalla condensazione tra diazoetano sostituito con un gruppo
2-nitrofenilico ed il nucleotide fosfato come tale. Il diazocomposto può essere prodotto
facilmente facendo reagire nitroacetofenone ed idrazina per formare il corrispondente
idrazone successivamente ossidato con MnO2:
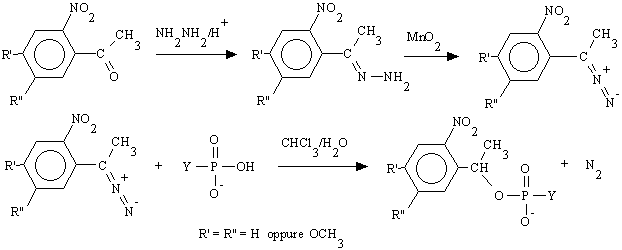
Per esteri fosforici debolmente acidi come ATP e analoghi, la reazione
finale viene condotta a bassi pH (circa 4) in solvente misto, generalmente
acqua/cloroformio, e può richiedere a seconda del composto fino a ventiquattro ore.
Sembra che questi tempi possano essere ridotti sostituendo il cloroformio con dietiletere.
Nel caso di composti più acidi, come i nucleotidi ciclici, è necessario l'uso di un
solvente omogeneo polare aprotico, generalmente dimetilsolfossido o dimetilformammide.
Questo perché probabilmente la reazione con il diazocomposto procede attraverso una forma
protonata dell'estere fosforico. La resa che si può ottenere con questo procedimento è
in alcuni casi, e con opportuni accorgimenti, vicina al 100% [97].
Grandi pregi di questo tipo di sintesi sono l'utilizzo dell'effettore come tale, del
gruppo di protezione in una forma facilmente ottenibile e la sua applicabilità generale a
composti contenenti un gruppo fosforico o un altro gruppo a carattere acido in grado di
reagire, sotto opportune condizioni, in modo analogo con il gruppo diazo. Sono stati ad
esempio sintetizzati in questo modo caged 6-fosfogluconato [89], caged inositolo
1,4,5-trifosfato (InsP3) [95], caged BAPTA [25] e caged fenilefrina [94] nei
quali i gruppi che reagiscono con la funzione diazo sono rispettivamente quelli fosforico,
nei primi due casi, carbossilico e fenolico. Possono inoltre essere facilmente ottenuti
caged compounds marcati radioattivamente [59, 89]. Ci sono però situazioni in cui questa
sintesi non è abbastanza specifica; ad esempio nella produzione di caged GTP(gS) il diazocomposto non discrimina tra atomi di O e di S del gruppo
tiofosforico [21] e nella sintesi di caged InsP3 reagisce con tutti e tre i
fosfati. Inoltre l'uso di 1-(2-nitrofenil)diazoetano comporta sempre la formazione di una
miscela di almeno due forme isomeriche per l'introduzione di un centro chirale sul
carbonio a del 1-(2-nitrofenil)etil derivato. Se in molti
contesti il prodotto può essere usato come tale per l'analogo comportamento fotolitico
delle forme isomere [21, 59], ci sono però situazioni in cui l'impiego di un isomero puro
è significativamente vantaggioso. La separazione cromatografica degli isomeri è
generalmente praticabile, ma in taluni casi è preferibile ricorrere ad un diverso e più
specifico procedimento sintetico [15].
Anche i caged Pi possono essere sintetizzati a partire da un diazocomposto
secondo lo schema precedente [97]; in alternativa vengono ottenuti mediante fosforilazione
della forma alcolica del gruppo di protezione. Tra i diversi metodi descritti [49, 58] il
più utilizzato si rifà allo schema proposto da Khwaja e coll. [53] ed in particolare
alla metodica indicata per la sintesi del 2-cianoetilfosfato da 2-cianoetanolo. L'alcool
di partenza viene fatto reagire con o-fenilene fosforocloridato in ambiente
basico per formare un diestere fosforico. Da quest'ultimo viene poi eliminata per idrolisi
la porzione o-idrossifenilica:
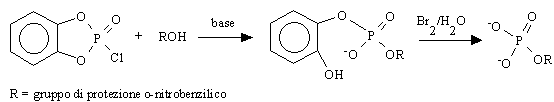
Questo metodo consente di ottenere in poche ore con buone rese
prodotti abbastanza puri. Il grado di purezza può comunque essere aumentato mediante
cromatografia su colonna di DEAE-cellulosa per ridurre la contaminazione da Pi
[63].
Un metodo generale per la sintesi di caged nucleotidi n fosfato (con n >
1) consiste nel produrre il corrispondente caged Pi e farlo poi reagire con una forma
attivata del nucleotide n-1 fosfato. Questo sistema viene attualmente impiegato per
ottenere 3,5-dinitrofenil ATP [15] e 3',5'-dimetossibenzoin ATP [91]. Diversi derivati
benzoinici del fosfato possono essere sintetizzati per fosforilazione del corrispondente
alcool con metildiclorofosfato [3]. Un metodo alternativo messo a punto di recente prevede
la fosforilazione del benzoino, in forma di chetale etilico ciclico, mediante reazione con
cianoetilfosforammidite seguita da ossidazione. L'eliminazione dei gruppi cianoetile per
trattamento con alcali in metanolo e l'idrolisi in ambiente acido del chetale forniscono
il prodotto desiderato. Quest'ultimo procedimento, anche se più complesso, è preferibile
in particolare quando si trattino benzoini asimmetrici in quanto minimizza la possibilità
di isomerizzazioni e formazione di prodotti collaterali [14].
1.2.2 Composti basici
Per quanto riguarda la possibilità di legare il gruppo o-nitrobenzilico a composti basici, due percorsi generali sono stati elaborati per la sintesi di derivati contenenti il gruppo amminico [11]. Uno di questi, applicabile però solo ad ammine primarie, prevede la trasformazione dell'ammina in isocianato e la successiva condensazione di questo con la forma alcolica del gruppo di protezione:
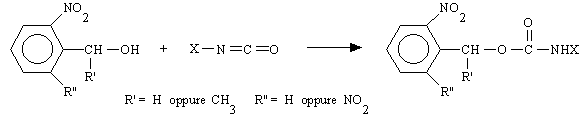
Nel secondo schema l'ammina, primaria o secondaria, senza dover essere modificata, viene fatta reagire con un nitrobenzilcloroformiato:
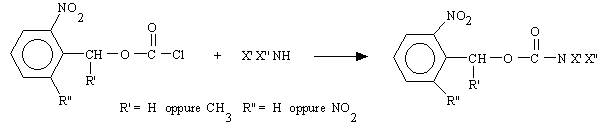
In questi casi tra l'effettore ed il gruppo di protezione è interposto
un gruppo carbossilico che viene rilasciato come CO2 contemporaneamente agli
altri fotoprodotti. Entrambe le metodiche precedenti sono state impiegate anche per la
sintesi di caged ammine fluorescenti [16].
Particolare, anche se da un punto di vista strettamente chimico analoga alla precedente,
è la reazione "centrale" impiegata nella sintesi della forma protetta di
diversi neurotrasmettitori agonisti dell'acetilcolina contenenti un gruppo amminico, in
particolare carbamilcolina. Questa consiste nella condensazione tra una
2-nitrobenzilammina e un cloroformiato, con formazione di un carbammato:
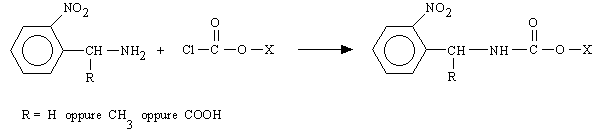
Il gruppo X varia a seconda dello specifico neurotrasmettitore e può essere modificato anche in una fase successiva alla reazione precedente [60, 96].
1.2.3 Amminoacidi
La preparazione di caged amminoacidi può essere effettuata legando il gruppo protettore alla funzione carbossilica o a quella amminica [74]. Più soluzioni sono state proposte per la sintesi degli esteri carbossilici per i quali, oltre ad una variante di quello più generale per i gruppi a carattere acido, sono state messe a punto due metodiche entrambe basate sulla reazione tra l'amminoacido e un bromoderivato del gruppo o-nitrobenzilico. Quest'ultimo viene ottenuto per riduzione con NaBH4 della corrispondente benzaldeide ad alcool seguita da reazione con PBr3 [100].
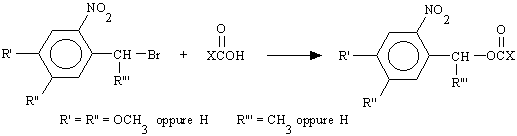
In un caso la reazione viene condotta in acetone in presenza di KF
[100], nell'altro in benzene e DBU (un diazobicicloundecene) [2]. Le diverse condizioni
impiegate rendono il secondo procedimento più rapido e semplice rispetto al primo. In
entrambi i casi le rese variano sensibilmente in base al gruppo protettore e soprattutto
all'amminoacido utilizzato.
Legare derivati nitrobenzilici direttamente al gruppo amminico degli amminoacidi sembra
essere più difficoltoso. Un procedimento descritto per la glicina prevede la formazione,
a partire da nitroacetofenone, di una nitrobenzilammina che viene poi fatta reagire con un
cloroacetato, il tutto in una serie di passaggi lunghi e complessi [100]. Un' interessante
alternativa da valutare in modo più approfondito consiste nella sintesi di caged
amminoacidi secondo le semplici procedure descritte precedentemente per altri composti
contenenti un gruppo amminico. Derivati nitrobenzilcarbonilici, come quelli che si
otterrebbero con tali metodiche sono stati introdotti da Patchornik [74] ed una caged
serina di questo tipo è stata impiegata in studi sul moto flagellare batterico [51].
Fattore comune di tutte le sintesi di caged amminoacidi è la necessità di proteggere
quei gruppi funzionali (quello amminico o quello carbossilico ed eventualmente altri
presenti sulla catena laterale dell'amminoacido) che non devono subire modificazioni nei
vari passaggi. Purtroppo la necessità di eliminare questa protezione come fase finale del
processo sintetico, in molti casi ne diminuisce sensibilmente le rese.
1.2.4 Protoni
Un caged H+, il 2-idrossifenil-1-(2-nitro)feniletil fosfato,
può essere sintetizzato seguendo la prima parte dello schema precedentemente indicato per
la fosforilazione degli alcoli [56]. Questo composto è infatti esattamente il prodotto
della reazione tra 1-(2-nitro)feniletanolo e o-fenilene fosforocloridato.
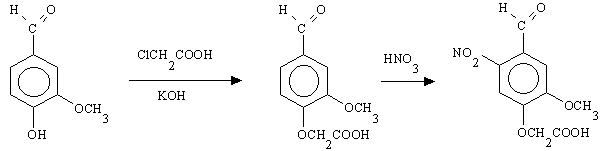
L'acido 4-formil-6-metossi-3-nitrofenossiacetico è un altro caged H+ che può
essere sintetizzato facilmente e con buone rese [45]. La sostanza di partenza è la
vanillina che trattata a caldo per alcune ore con KOH e acido cloroacetico forma acido
4-formil-2-metossifenossiacetico; l'acido cloroacetico reagisce infatti facilmente con i
fenoli in soluzioni acquose di alcali. Il composto prodotto, previa acidificazione della
miscela di reazione con HCl concentrato, può essere raccolto per filtrazione e facilmente
purificato per ricristallizzazione. Dalla successiva nitrazione per trattamento con acido
nitrico e acido nitrico fumante prima a 0 °C e poi a temperatura ambiente si ottiene il
caged H+. Infatti, quando il gruppo alcolico della vanillina è bloccato per
eterificazione o per esterificazione, la sostituzione sull'anello aromatico avviene
preferibilmente in posizione orto rispetto al gruppo formilico. Anche il prodotto finale,
dopo raffreddamento della miscela con ghiaccio, viene raccolto per filtrazione e
successivamente ricristallizzato in etanolo:
1.2.5 Ioni calcio
Per i caged Ca++ della serie nitr la reazione cardine è quella tra la forma esterificata del BAPTA e una nitrobenzaldeide o un corrispondente acetale; per il successo di questo passaggio è necessaria la presenza, nella miscela di reazione, di trimetilsilil trifluorometansolfonato come attivatore.
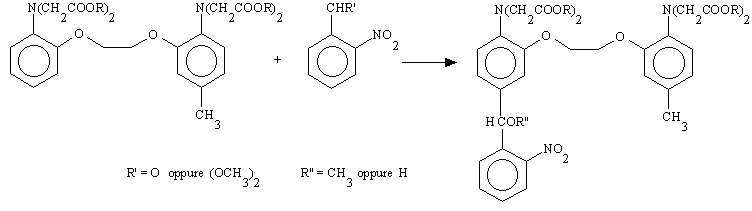
A seconda dell'elemento della serie possono essere presenti diversi
sostituenti sull'anello benzilico ed in alcuni casi, nitr-4 e nitr-7, anche sull'etile del
BAPTA [1].
Nella sintesi del DM-nitrofen la molecola viene costruita in passaggi successivi a partire
da una forma modificata del gruppo protettore [23].
1.2.6 Purificazione e conservazione
I caged compounds sintetizzati in alcuni casi possono essere isolati
per cristallizzazione, ma più frequentemente vengono utilizzate tecniche cromatografiche
ed in particolare HPLC. Per gli esteri fosforici l'ultimo passaggio, che può essere
l'unico se non è richiesta un'elevata purezza, è generalmente una cromatografia su
colonna di DEAE-cellulosa eluita con un gradiente lineare di bicarbonato di trietilammonio
che fornisce il composto in forma di sale trietilammonico, forma nella quale viene
conservato.
Il composto isolato può essere caratterizzato mediante tecniche di NMR,
spettrofotometriche (in particolare UV), analisi chimica elementare e caratteristiche
fisiche. Un test specifico consiste nella fotolisi del caged dalla quale si deve
naturalmente ottenere l'effettore proprio.
Va infine ricordato che un numero sempre maggiore di caged compounds è disponibile
commercialmente. Questi prodotti possono presentare impurezze da effettore libero a cui si
può ovviare purificandoli cromatograficamente [50].
La conservazione dei caged compounds viene effettuata generalmente a basse temperature
(-15, -20 °C) e al buio.